L'aspirine est l'acide acétylsalicylique,

on le prépare à partir d'acide salicvlique
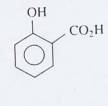
et d'anhydride acétique
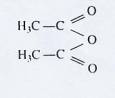
Ä réaliser une étape de la synthèse industrielle de l'aspirine
Ä purifier un produit par recristallisation
|
L'aspirine est l'acide acétylsalicylique,
|
on le prépare à partir d'acide salicvlique
|
et d'anhydride acétique
|
1. Dans un erlenmeyer de 125 mL sec, introduire 5 g d'acide salicylique puis muni de gants et de lunettes 6 mL d'anhydride acétique mesurés à l'éprouvette. Ajouter 3 à 4 gouttes d'acide sulfurique à l'aide d'un compte gouttes et avec précaution. Adapter un réfrigérant à boules et chauffer au bain-marie maintenu entre 50 et 60°C (thermostat sur 110°C) pendant 10 à 15 minutes tout en agitant avec l'agitateur magnétique.
2. Après le chauffage, ajouter par le sommet du réfrigérant par petites portions successives 5 mL d'eau, en agitant toujours et en prenant garde aux vapeurs chaudes et acides, puis deux fois 20 mL d'eau glacée. Placer ensuite l'erlenmeyer dans de la glace jusqu'à ce que la cristallisation soit complète.
3. A l'aide d'un agitateur en verre, écraser les grumeaux qui ont pu se former et filtrer sur büchner en tirant sous vide à l’aide de la trompe à eau. Interrompre la trompe à eau lors du lavage des cristaux avec un peu d'eau froide avec laquelle on rince l'erlenmeyer. Aspirer de nouveau.
4. Dans un erlenmeyer propre, transférer les cristaux en vue de leur recristallisation. En garder une pointe de spatule que l'on placera dans un tube à essais en vue du test réalisé dans la partie. La recristallisation a pour but de purifier un produit en le débarrassant des impuretés organiques ou minérales qu'il pourrait contenir. Cette technique repose sur la différence de solubilité, dans un solvant donné, entre le produit pur et ses impuretés : on dissout le produit brut dans le minimum de solvant à chaud. Par refroidissement, le produit cristallise seul en laissant les impuretés en solution dans le solvant, il faut donc choisir un solvant ou un mélange de solvants dans lequel :
- le produit est peu soluble à froid
- les impuretés restent en solution à froid.
Ajouter au contenu de l'erlenmeyer 5 mL d'éthanol et le chauffer sur la plaque chauffante (thermostat 140°C) en agitant, jusqu'à dissolution complète. Ajouter alors 15 mL d'eau chaude. Si la solution se trouble, chauffer sur la plaque chauffante jusqu'à obtenir une solution limpide. Laisser refroidir ensuite lentement à température ambiante, puis ensuite dans un bain de glace, sans agiter.
5. Filtrer les cristaux formés sur büchner et laver avec un peu d'eau glacée. Récupérer les cristaux dans un verre de montre que l'on aura préalablement pesé. Mettre à l'étuve à 80 °C pour sécher. Peser le produit obtenu lorsqu'il est sec.
6. Vérification de la pureté du produit obtenu : on réalisera le test de recherche d'impuretés phénoliques : Placer quelques cristaux du produit recristallisé dans un tube à essai propre : les dissoudre dans quelques mL d'eau distillée froide puis ajouter 1 mL d'une solution diluée de chlorure de fer (III). Noter vos observations.
Remarque: les ions Fe3+ donnent avec la fonction phénol de l'acide salicylique un complexe violet.
Faire le même lest avec l'échantillon prélevé avant la recristallisation et avec un échantillon d'acide salicylique.
Faire les schémas du montage de préparation et de la filtration sous vide.
Déterminer la quantité d'acide salicylique mise enjeu ainsi que celle d'anhydride éthanoïque de masse volumique µ= 1,08 g.cm-3. Ecrire l'équation bilan de la réaction. Quel est le réactif limitant ?
Indiquer la masse de produit recristallisé sec obtenu et calculer le rendement de la réaction de préparation.
Calculer le rendement de la réaction.
Donner le résultat des tests effectués avec la solution de chlorure de fer (III). Conclure.