NOM :
Prénom :
Contrôle de sciences physiques
2nde 5
Physique
|
Qu’appelle-t-on phénomène de réfraction ? Quelle observation de la vie courante attribue-t-on à ce phénomène ? M. Hulot est en vacances au bord de la mer. Il marche tranquillement dans l'eau peu profonde lorsque tout à coup, il remarque qu’il est sur le point de poser le pied sur un oursin. "Heureusement, pense-t-il, je l'ai vu à temps pour l'éviter". Mais au moment où il pose le pied sur ce qu’il croit être le sable, il ne peut retenir un cri de douleur. Il a bel et bien marché sur l'oursin : la réfraction de la lumière a dévié l’image qu’il avait de l’oursin. On a représenté un rayon lumineux issu de l’oursin qui va parvenir jusqu’à l’œil de M.Hulot. Tracer, sans faire aucun calcul, un cheminement possible de ce rayon hors de l’eau. Le rayon représenté fait un angle d’incidence de 20°. Placer cet angle sur la figure. Définir l’indice de réfraction d’un milieu transparent. Quel est l’indice du milieu 1 ? Calculer l’angle de réfraction, lors de ce changement de milieu . Compléter le schéma et expliquer pourquoi Mr Hulot a marché sur l'oursin Donnée : n air = 1 ; n eau = 1,33
|
0.5 1 |
0.5 0.5 0.5 |
0.5 1.5 1 |
|||||||||
|
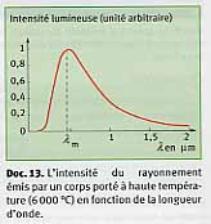
II. Etude de document : En déplaçant un photorécepteur le long d’un spectre lumineux obtenu par décomposition de la lumière émise par une source chaude portée à une température T, on a mesuré la répartition de l’intensité lumineuse I en fonction des longueurs d’onde l du spectre. La représentation graphique I = f(l) présente un maximum pour une longueur d’onde lm qui dépend de la température T de la source lumineuse. La loi qui relie lm à T est connue sous le nom de « loi de Wien » elle s’écrit sous la forme lm.T = A (où A est une constante qui vaut 2,9.103 µm.K). Le symbole K est celui du Kelvin, unité de température qui se déduit du degré Celsius par la relation : température T(en K) = température q(en degré Celsius) + 273 Le graphique ci dessous est obtenu pour une source portée à 6000°C. |
|
|
|
|
||||||||
|
Expliquer ce que représente l ? Quelle est son unité dans le système international ? Dans quelle unité doit-on exprimer lm pour calculer la constante A donnée dans le texte ? Quelle est, en K, la température de la source lumineuse ? Vérifier par le calcul la valeur de A donnée dans le texte. Comment pourrait-on expérimentalement vérifier la loi de Wien ? (Proposer une méthode) |
1 0.5 |
0.5 1 |
2 |
|||||||||
|
Chimie: I. Décrire la structure d’un atome en utilisant les mots : noyau, électrons, protons, neutrons. 1.5 2 II. Le noyau d'un isotope de l'atome de cobalt peut être représenté par 5927Co . Quelle est la composition de cet atome? On le compare à l'atome X dont le noyau est caractérisé par 5928X. ces deux noyaux sont-ils isotopes ? 1 III. L’acétate d’isoamyle est une espèce chimique odorante présente dans les bananes. Sa formule chimique est C7O2H14. La molécule d’acétate d’isoamyle est-elle une espèce chimique artificielle ? Justifier la réponse. On peut l’extraire en utilisant l’entraînement à la vapeur. On verse ensuite le distillat obtenu dans une ampoule à décanter, on le lave avec de l’eau salée et on extrait l’acétate d’isoamyle du distillat par solvant. Parmi les solvants cités dans le tableau ci-dessous, lequel faut-il utiliser pour extraire l’acétate d’isoamyle ? Justifier la réponse. Faire un schéma de l’ampoule à décanter en justifiant la nature de chacune des phases. |
1 1 0.5 |
1 1 |
1.5 |
|||||||||
|
|
Densité |
Solubilité dans |
|
|||||||||
|
|
Eau |
Eau salée |
Cyclohexane |
Acétone |
|
|||||||
|
Eau |
1,00 |
Infinie |
Infinie |
Nulle |
Importante |
|
||||||
|
Acétate d’isoamyle |
0,87 |
Faible |
Nulle |
Importante |
Importante |
|
||||||
|
On peut également synthétiser l’acétate d’isoamyle au laboratoire. Pour cela, on mélange dans un ballon 30 mL d’acide acétique et 22 mL d’alcool isoamylique. On y rajoute 2 mL d’acide paratoluène qui sert de catalyseur et quelques grains de pierre ponce. On chauffe à reflux pendant une heure. On lave le mélange obtenu à la fin de la réaction et on effectue une chromatographie. La plaque obtenue après révélation est représenté ci-dessous. Le mélange H obtenu après hydrodistillation est-il pur ? Justifier la réponse ? Obtient-on de l’acétate d’isoamyle lors de la synthèse au laboratoire ? Justifier la réponse. La synthèse consomme-t-elle tous les réactifs ? Justifier la réponse.
C : acétate d’isoamyle du Commerce A : Alcool isoamylique H : mélange obtenu après Hydrodistillation S : mélange obtenu après Synthèse au laboratoire |
|
|
1 1 1 |
|||||||||
Exercice 1 (14
points)
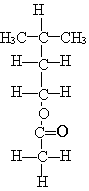
L’acétate d’isoamyle est une espèce chimique odorante présente dans les bananes. Il est représenté ci-contre.
On peut l’extraire en utilisant l’entraînement à la vapeur. On verse ensuite le distillat obtenu dans une ampoule à décanter, on le lave avec de l’eau salée et on extrait l’acétate d’isoamyle du distillat par solvant. |
|
- Parmi les solvants cités dans le tableau ci-dessous, lequel faut-il utiliser pour extraire l’acétate d’isoamyle ? Justifier la réponse.
|
|
Densité |
Solubilité dans |
|||
|
|
Eau |
Eau salée |
Cyclohexane |
Acétone |
|
|
Eau |
1,00 |
Infinie |
Infinie |
Nulle |
Importante |
|
Acétate d’isoamyle |
0,87 |
Faible |
Nulle |
Importante |
Importante |
|
Acide acétique |
1,05 |
Infinie |
Infinie |
Faible |
Importante |
|
Alcool isoamylique |
0,81 |
Très faible |
Nulle |
Importante |
Importante |
- Faire un schéma de l’ampoule à décanter en justifiant la nature de chacune des phases.
On peut également synthétiser l’acétate d’isoamyle au laboratoire. Pour cela, on mélange dans un ballon 30 mL d’acide acétique et 22 mL d’alcool isoamylique. On y rajoute 2 mL d’acide paratoluène qui sert de catalyseur et quelques grains de pierre ponce. On chauffe à reflux pendant une heure.
- Qu’est-ce qu’un réactif ?
- Qu’est-ce qu’un produit ?
- Qu’est-ce qu’un catalyseur ?
- A quoi sert un chauffage à reflux ?
- Faire le schéma du montage utilisé.
On sépare le mélange obtenu en deux parts égales. Dans la première, le pH mesuré est égal à 2 et on y ajoute quelques grammes de sulfate de cuivre anhydre qui bleuit au contact du mélange.
- Quelle(s) conclusion(s) peut-on tirer des tests effectués sur la première partie du mélange ? Justifier la réponse.
- Citer deux méthodes de caractérisation d’espèces chimiques ?
On lave la deuxième partie du mélange et on effectue une chromatographie. La plaque obtenue après révélation est représenté ci-contre.
|
|
C : acétate d’isoamyle du Commerce A : Alcool isoamylique H : mélange obtenu après Hydrodistillation S : mélange obtenu après Synthèse au laboratoire |
|