TS2 Correction du contrôle n°1
PHYSIQUE
Exercice n°1 : Propagation d’une onde
le long d’une corde
La règle mesure 1 mètre de long. La corde est
posée sur un sol lisse. On imprime une secousse brève à l'un de ses extrémités.
A l'aide d'un caméscope , on filme la propagation de la perturbation le long
de la corde. Quelle est la nature de l'onde ?
L’onde mécanique est transversale, sa direction de propagation
est perpendiculaire à celle des points de la corde affectés par la perturbation.
1.
De quelle distance l'onde s'est-elle propagée entre
les instants t1et t3 ?
A l’instant t1, le front de l’onde
est au milieu de la règle, à l’instant t3, le front de l’onde est
à 15 cm de l’extrémité de la règle. Entre les 2 instants, l’onde a parcouru :
50-15 = 35 cm
En déduire la célérité de l'onde
.
La célérité de l’onde est c = d/(t3-t1) = 35.10-2/(0,71-0.25).
C = 0,76 m.s-1
2.
A quelle date l'onde atteint-elle le point B (extrémité
de la règle) ?
A la date t3, il reste d = 15 cm
à parcourir à l’onde pour arriver à l’extrémité. Sa célérité est C = 0,76 m.s-1
Il lui faudra une durée t = d/C = 0,15/0,76 = 0,20 s après t3.
L'onde atteindra
le point B à la date t4 = t3 + t = 0,71 + 0,20 = 0,91
s
Exercice 2 : Mesure de la célérité
des ultrasons
|
Un émetteur émet des ultrasons par salves.
Un récepteur est placé au voisinage de l’axe d’émission. Les oscillations
des tensions émises et reçues sont visualisées respectivement sur les
voies 1 et 2 d’un oscilloscope.
La sensibilité du balayage est b = 0,10
ms/div.
Schéma du dispositif expérimental.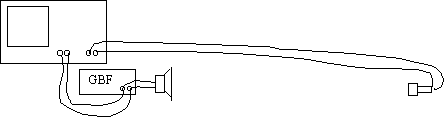
Période et la fréquence des ondes ultrasonores :
Sur 1 division horizontale, on observe 4 périodes
de l’onde, donc T = 0,1/4 =0,025 ms
|

La salve émise s’étale sur N=5 divisions
horizontales. Sa durée est donc de N.b = 5.0,1 = 0,5 ms
|
La fréquence F = 1/T = 1/(0,025.10-3)
= 4.105 Hz
La distance séparant l’émetteur et le récepteur est D = 171 mm.
La célérité des ondes ultrasonores dans l’air ambiant est c = D/t. t est le retard entre l’émission et la réception. t représente
5 divisions soit 0,5 ms. c= 171/0,5 = 342 m/s
Expression de la longueur d’onde d’une onde progressive
périodique en fonction de sa fréquence et de sa célérité dans le milieu de propagation
l = c/F. Analyse dimensionnelle :
c en m/s ; F en Hz (s-1) donc l en (m.s-1)/(s-1)
soit en m (unité de longueur).
l = 342/40000 = 0,00684 m = 8,55 mm
CHIMIE
Exercice 3 : Action de l'acide
chlorhydrique sur le zinc
On fait réagir une solution d'acide chlorhydrique
sur du magnésium solide selon la réaction :
2 H3O+(aq) +
Mg(s) ® H2(gaz) + Mg
2+(aq) + 2 H2O
A t = 0, on introduit une masse m = 0,5 g de magnésium dans un volume VA
= 20 cm3 d'acide chlorhydrique à la concentration CA =
1,0 mol. L-1 . La température du milieu réactionnel est égale à
q = 20°C . On mesure le volume VH2 de dihydrogène
formé au cours du temps.
Les couples mis en jeu sont :
Mg2+(aq) / Mg(s) et H3O+(aq) / H2(gaz)
Tableau d'avancement
| |
2 H3O+(aq)
+
|
Mg(s) ®
|
H2(gaz)
|
+ Mg 2+(aq)
|
+ 2 H2O
|
|
Etat initial
|
n1 = CA.
VA
=2,0.10-2 mol
|
n2 = m/M
= 2,0.10-2 mol
|
|
|
|
|
avancement
|
n1 – 2x
|
n2 - x
|
x
|
x
|
2x
|
|
xfinal = min(n1/2 ;
n1)
|
0
|
1,0.10-2 mol
|
1,0.10-2 mol
|
1,0.10-2 mol
|
|
Le réactif limitant est H3O+
Concentration en ions Mg2+ lorsque
l’avancement final est atteint :
A l’avancement final : n(Mg2+)
= xfinal
donc [Mg 2+] = xfinal
/ VA =1,0.10-2 / 20.10-3 mol = 0.5 mol/L
Relation entre le volume de dihydrogène VH2
mesuré à un instant t et la concentration en ions Mg2+ à ce même instant. On
notera Vm le volume molaire des gaz : A l’instant t, n(Mg2+) = n(H2) = xfinal ; or n(Mg2+)= [Mg 2+].VA et
n(H2) = V(H2)/Vm ; d’où [Mg 2+].VA
= V(H2)/Vm
On a donc : [Mg 2+] =
V(H2 )/(Vm.VA)
Mesure du volume de dihydrogène dégagé
en fonction du temps :
|
t (s)
|
0
|
100
|
200
|
400
|
600
|
800
|
|
V(H2) L
|
0
|
0,096
|
0,148
|
0,192
|
0,23
|
0,23
|
[Mg 2+] = V(H2
)/(Vm.VA)
|
t (s)
|
0
|
100
|
200
|
400
|
600
|
800
|
|
[Mg 2+] mol.L-1
|
0
|
2.10-1
|
3.10-1
|
4.10-1
|
4,8.10-1
|
4,8.10-1
|
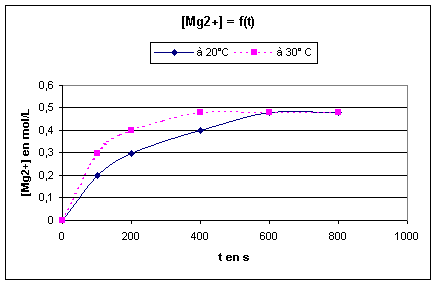
Allure de la courbe [Mg2+] = f (t) (en bleu).
Etat initial 0 mol/L; état final limite
0,5 mol/L (concentration attendue pour xfinal)
Allure de la courbe [Mg2+] = f(t) que l'on obtiendrait à la température
q = 30 ° C (en rose pointillés), même état final atteint
plus rapidement.